外科手術とカテーテル治療の長所短所を見極めながらの第5回JES:
史上最多参加者755名と共にやりきった渾身の23例
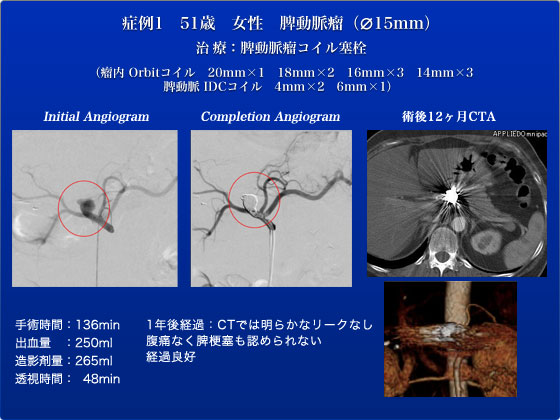
症例1は径15mmの嚢状脾動脈瘤でした。動脈瘤の前後でinflowとoutflowも塞栓するため左右の大腿動脈を穿刺して右に6Frシース、左に5Frシースを留置しました。Outflowのコイル塞栓は脾動脈瘤のコイル塞栓を行い、末梢への血流が減少した時点で塞栓する方針としました。そうしないと末梢側のコイルが血流で流されてしまう可能性があるからです。左大腿動脈からRenegadeマイクロカテーテルを脾動脈瘤末梢まで挿入した後に、右大腿動脈から6Fr RDC1ガイディングカテーテルを腹腔動脈根部に留置し、Prowlerマイクロカテーテルを脾動脈瘤内に留置しました。脾動脈のコイルが流されないように、先ず脾動脈瘤をOrbitマイクロコイル9本を用いて塞栓して脾動脈瘤末梢への血流が減少した後に、Renegadeマイクロカテーテルで脾動脈outflowをIDC-18コイル1本にて閉じ、そして、最後に脾動脈瘤流入血管をIDC-18コイル2本にて閉じました。術後、脾梗塞の所見もなく経過良好で第3病日で退院となっています。術後1年経た現在も経過良好です。
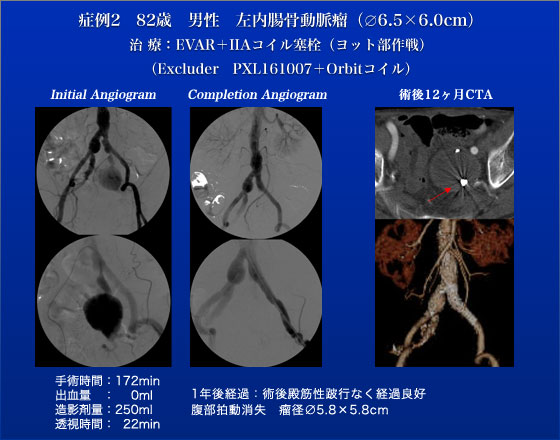
症例2は82歳、男性、左内腸骨動脈瘤(∅65×60mm)です。腹痛を主訴に近医でCT検査を行い、左内腸骨動脈瘤を指摘されましたが、複数の開腹手術歴および慢性閉塞性肺疾患(COPD)があることから、ステントグラフトによる治療目的に当院紹介となった患者です。右大腿動脈を穿刺し、crossoverで左内腸骨動脈瘤内までカニュレーションを行いました。水圧式デタッチャブルコイルのOrbitを瘤内で展開し、血流に任せてoutflow vesselに流れ込んだ時点でコイルをdetachするといういわゆる「ヨット部作戦」でoutflowをコイル塞栓しました。コイル塞栓後にステントグラフトを総腸骨動脈から外腸骨動脈にかけてdeployし内腸骨動脈瘤の空置に成功しました。術後経過は良好で、殿筋跛行も認めず、術後2日目に退院しました。1年後のCTでも瘤は縮小傾向でエンドリークも認めません。
(CodmanのClinical Updateに「Trufill DCS Orbitを用いたテクニック」として本症例が掲載されております)
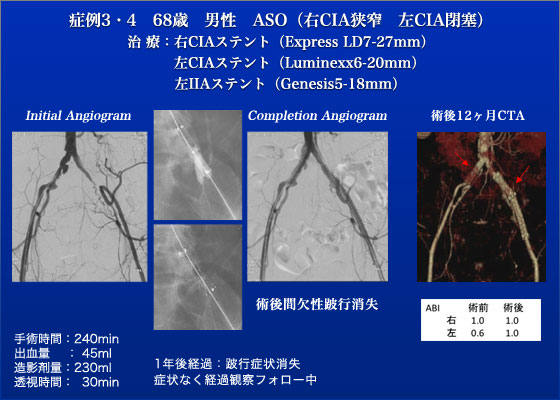
症例3、4は閉塞性動脈硬化症の患者で、右総腸骨動脈狭窄と左総腸骨動脈の閉塞を認めていました。症状は200mの間歇性跛行であり、まず内服療法を開始しました。当初プラビックスの治験を行っており、約1年間の内服で跛行距離が500mまで改善しましたが、本人のもっと長い距離を歩きたいという強い希望により手術を行う方針としました。
治療はまず右大腿動脈に6Frシースを挿入し大動脈造影を行い、roadmapを使用しながら対側の左大腿動脈にもシースを挿入しました。まず対側のCTO病変に対してはRDCガイディングシースを挿入し山越えでアプローチすると共に同側からもアプローチを加えました。同側から0.014" AstatoワイヤにてCTOを突破し4×20mmのSterlingバルンにて前拡張しました。その後ステントの挿入を考えましたが、プラークシフトによる内腸骨動脈の閉塞が考えられたため、対側からXtremeワイヤを挿入し、内腸骨動脈にもステントを挿入することでkissingステントとしました。総腸骨動脈に6×30mmのLuminexxステント、内腸骨動脈には5×18mmのPalmaz Genesisステント(PG1850PMW)を使用しました。追加で圧較差を認めた右の総腸骨動脈に7×27mmのExpress LDステントを挿入しました。最終造影で術中に大動脈への逆行性解離を認めましたが、術後の腰背部痛などは認めず、CTにて限局性解離であることを確認し退院となりました。1年後の経過では術前に認めた跛行症状は完全に消失しており、全てのステントは開存しています。また限局性解離は血栓化して、治癒しております。
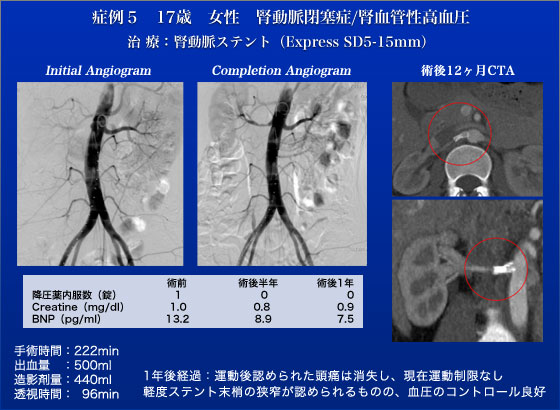
症例5は17歳、女性で、他院にて高安動脈炎(大動脈炎症候群)の診断のもとステロイドを内服していた若年患者です。右腎動脈が閉塞しており、降圧剤内服も、コントロール不良で、運動後に頭痛が出現するため、運動することを医師に止められておりました。腎動脈のCTOというchallengingな症例ですが予想通り、右腎動脈の閉塞部をcrossするのに難渋致しました。まず右総大腿動脈から挿入した6FrRDCガイディングシースから、様々なカテーテル、ガイドワイヤーを用いましたが、通過せず、予定の倍以上のライブタイムを使ってしまった上に術中大動脈穿孔を起こした際は多くのコメンテーター等から撤退すべきと指摘されました。しかしこの未婚の女の子にステント術が成功しなかったからと言ってすぐさま開腹バイパス術を行う訳にもいきませんが、かと言ってずっと運動ができないのもかわいそうですので、ライブプログラムのスケジュールを無視して手技を継続しました。大腿動脈からのアプローチである程度CTOを掘り進めた後に右上腕動脈からのアプローチを試みたところ、閉塞部を何とか突破する事ができました。5Fr shuttleシース補助下でExpressSD5-15を留置し、やっとの思いで血行再建を完遂しました。辛抱強くお付き合いいただいた皆さんに感謝します。術後、腹痛の訴えなく、降圧剤の内服を中止とし退院の運びとなりました。術直後から運動後の頭痛も消失したため、運動制限も完全に解除され、待ちに待った部活を再開できたと本人も家族もとても喜んでいました。1年目の定期検査で、ステントの末梢側に、軽度の残存狭窄が認められていますが、降圧剤無しで血圧のコントロールは良好であり、現在高校三年生になった患者はボート部の活動を満喫し、そろそろ受験勉強をはじめるとの事です。術後1年目検診の際に青春を取り戻した彼女の笑顔を見た時、頑張って完遂して良かったと心から思いました。内膜剥離術という選択肢のある頸動脈狭窄症や、バイパス術ができる浅大腿動脈閉塞症に対するカテーテルインターベンションにおいてはステントでの深追いは禁物ですが、このような手術が施行困難で、かつ病変を放置できない症例においてはとことん追求する価値があると思います。インターベンションの治療においては術中の外科手術のリスク評価とそれに照らしてインターベンション追及のさじ加減を決める事が大事であることを本症例は教えてくれています。本ライブのハイライトの症例の一つと言えるでしょう。
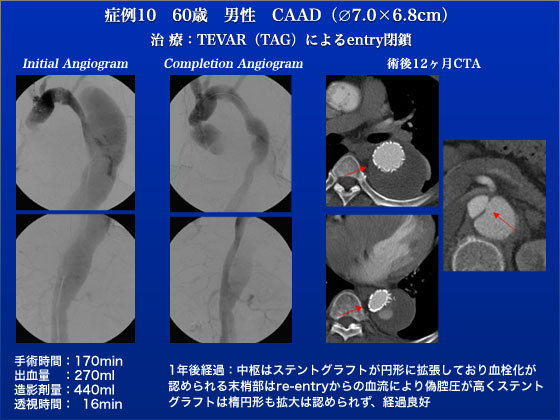
症例6は76歳、女性の腹部大動脈瘤患者です。胸部下行大動脈がshaggyな上に中枢neckの径が12mmと細めであるためまず自作のステントグラフト(Palmaz+PTFEグラフト)でneckを作成して(neck builder)、Excluderで治療する予定としました。しかし、実際にはこの自作ステントグラフトが目的位置まで上がらずに通常のExcluderで治療を行ないました。途中で左腎動脈の塞栓と思われる閉塞がみられましたのでステントグラフト挿入後に左大腿動脈からANSEL2のシースを挿入して左腎動脈をスターリング4-20で拡張した後にpalmaz Genesis15-15(PG1550PMW)をdeployして腎臓の救済を行ないました。術後腎機能の悪化も認めずに退院しました。術後1年のCTでもエンドリークを認めず経過良好です。胸部下行大動脈がshaggyなため先端のfloppyな部分が1cmのアンプラッツwireを用いて胸部下行大動脈には深くwireを挿入せずにステントグラフト手術を行ないましたがこういう症例には先端に長いダイレーターがなくかつSupra-renal stentがないExcluderが安全であります。
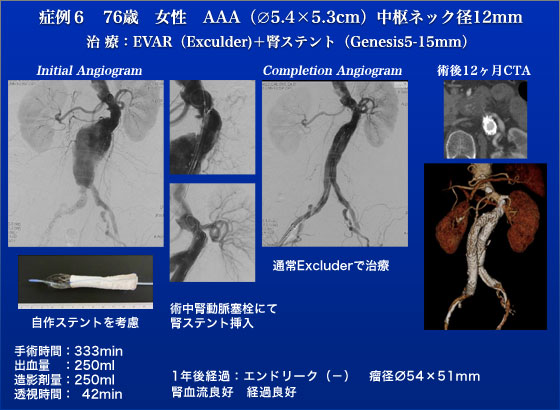
症例7、8は79歳の男性で左SCAを巻き込む遠位弓部大動脈瘤です。術前のCTAで左VAが大動脈より直接分枝していたため、左SCAをcoverした後に、SCA-SCA bypassが場合によっては必要と考えていました。まず血管造影にて、左VAが大動脈より直接分枝していることを確認。頸動脈造影を行いますと、左内頸動脈は狭窄しており、右内頸から左前・中大脳領域がすべて造影されていました。アクセス不良のため、後腹膜経路による右CIAアプローチでTalent(Xcelerant)を挿入しました。既存Talentは当時まだCoilTrackデリバリーシステムで弓部など屈曲部でのアンシースが困難であるという問題点があり、全国的に普及しにくい状況でありました。そこで登場したのがこのXcelerantでこれは従来の製品よりも弓部のような屈曲部でもdeployがスムースに行われるよう改良されており、ATPで心臓は停止させましたが、スイスイ正確にdeployすることができました。弓部瘤でありながらBird Beakも見られずナイスフィットでした。術後脳梗塞もなく元気に退院されています。この症例は「弓部だからこそTalent」という典型的な症例と言えます。なお症例8は本症例に腋窩‐腋窩動脈バイパスを付加する予定でしたが術中判断で行わないことにしました。術後患者は消息不明となってしまいました。
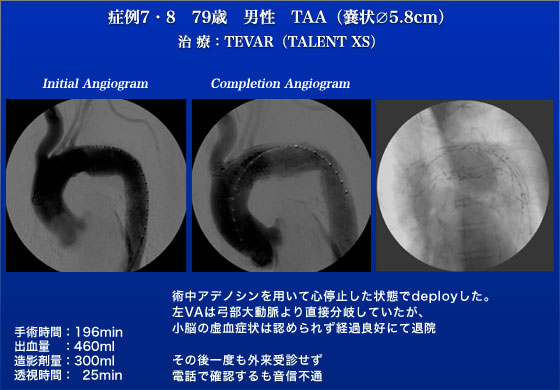
症例9は83歳の男性で、左鎖骨下動脈を巻き込む形で存在する68mmの嚢状胸部大動脈瘤です。Bovine typeの大動脈弓は急峻であった為に、Comfarmable-TAG(C-TAG)での治療を選択いたしました。TEVARに先立ち、左右のVA造影を行うと、右VAがCTOで左VA dominantで小脳が造影されました。末梢SGを留置した後に、中枢SGを左鎖骨下動脈カバー、腕頭動脈に合わせて留置しましたが、留置時に前方にjumpingして腕頭動脈を1/3カバーする形となってしまいましたが、左右の総頸動脈を左右差なく良好に触知した為、追加処置を行いませんでした。中枢SG挿入時に末梢SGがmigrationしてしまったので、末梢にSGを追加致しました。確認造影で、後交通動脈を介して小脳が造影された為、鎖骨下_鎖骨下動脈バイパスは行わない方針とし、左鎖骨下動脈コイル塞栓術を行いました。若干のエンドリークが残った状態で手術終了となりましたが、術後1年経過しエンドリークなく瘤が空置されており、左手虚血症状、脳梗塞発症もなく経過良好です。TAGはこの当時も現在も良く使用されている胸部用のdeviceですが屈曲部に留置すると小弯側が浮き上がった形となるいわゆるBird Beakが弱点の一つです。このC-TAGはその弱点を改良したものでC-TAGの利点を示すために弓部の屈曲の強い症例を選びましたが見事にarchにフィットしております。
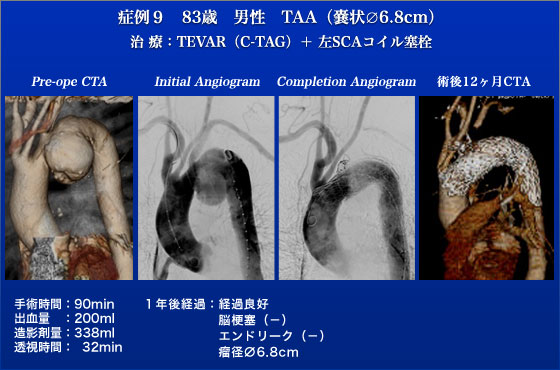
症例10は60歳、男性。大動脈解離で弓部置換術後を受けています。残存する慢性解離性大動脈瘤の中枢側の tearのみをTAGにて閉鎖しました。TAG留置後、腹部のsecondary tearから頭側に血流が向かうようになり、手術終了としました。術後対麻痺なく、経過良好で退院となっています。術後1年のCTでは、primary tearでのエンドリークは見られず、偽腔は血栓化しステントグラフト中枢は円形に拡張しています。ステントグラフト末梢はre-entryからの血流により偽腔圧が高くステントグラフトは正円ではなく楕円形を呈していますが、偽腔圧が極めて高い時に見られる凹サインが見られない上に瘤径は6.8cmと大きさに変化無く、経過観察中です。今後、瘤のサイズアップを認めるようであれば、secondary tearの治療を考慮したいと思います。Stanford Bの解離やStanford Aで上行弓部置換を行った後の残存解離などによる慢性解離性大動脈瘤にたいするステントグラフト治療は全てがステントグラフトの対象となるわけではありませんがこういったtearと動脈瘤の最大径が近く、secondary tearとの間が離れているような症例では瘤の拡大を防ぐことが出来ると考えております。
症例11は67歳、男性で右頸動脈狭窄の症例です。もともと両側頸動脈狭窄(左99%、右70%狭窄)であり、左頸動脈は症候性(左脳梗塞)であったため、2010年4月にCEAを行いました。右頸動脈に対しては、頸動脈狭窄病変がC2 と高位でありCEAは行いづらいため、頸動脈ステント術を選択しました。まず、脳血管造影と頸動脈造影を行ない、左CEA部の狭窄のないことと右内頸動脈80%狭窄を確認しました。つづいて、ガイディングシース(6Fr Destination)を右総頸動脈に留置しました。右内頸動脈狭窄部は、日本で新たに認可された頸動脈塞栓防止デバイスであるFilter wireを使用し、Carotid wall stent (10×24mm)を内頸動脈から総頸動脈にかけて留置しました。Filter wireの回収時にステントにひっかかりましたが、頸部を用手的に圧迫するテクニックを用いて問題なく回収されました。filter内には微小プラークは認めず、脳血管造影で術後前大脳動脈の造影効果が良好で脳梗塞を疑わせる所見もありませんでした。現在まで脳梗塞の発症はなく、1年後の評価でもCEA部、ステント部とも再狭窄は認めておりません。この症例の様に同一患者であっても頸動脈分岐の位置や頸動脈病変の位置や、性状によってCASとCEAを使い分けることも重要です。
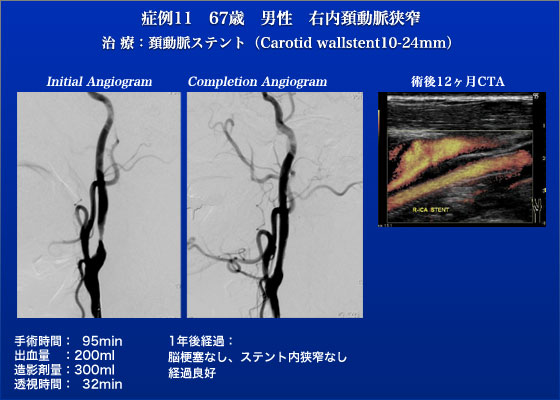
症例12、13は79歳、男性でAAAと両側頸動脈狭窄、右腎動脈狭窄で経過観察中に難治性高血圧のためまず腎動脈ステントと左頸動脈ステントが行なわれております(2010年3月)。今回は右の頸動脈狭窄とAAAの治療を行ないました。まず、右頸動脈のCEAを行ないました。右内頸動脈は屈曲が著明でCEAを選択しました。3cmの小切開で頸動脈を総頸から内外頸動脈に至るまで露出して、総頸動脈遮断後にeversion法で内頸動脈のプラークを摘出しました。プラーク長は35mmでした。切除後に屈曲を解除するように内頸動脈を一部切除して再吻合しました。我々は頸動脈狭窄の侵襲的治療の第一選択はCEAと考えていますがCEAはこの様に頸動脈の屈曲した症例にも対応可能であり、かつ屈曲を是正することもできるため非常に有用であると考えています。まさにこのeversion法のCEAの利点が凝集された症例といえるでしょう。
次いで、AAAについてはZenith Flexを用いて治療を行ないました。3月にdeployされていた腎動脈ステントに狭窄はありませんでした。屈曲した腸骨動脈でしたがZenith Flexは屈曲に追従して挿入可能でした。左の腸骨動脈の屈曲に対しては体外からの用手圧迫とpush&pullテクニックでdeviceの挿入を行ないましたが、外腸骨動脈の一部に解離を認めたためSMARTステントをdeployしました。
CEAとAAAの同時手術でしたが術後脳梗塞もなく元気に退院され、術後1年の時点でもエンドリーク無く良好に経過しております。この症例は元々腎動脈狭窄症の治療目的に紹介されましたが、終わってみればそれ以外に両側頸動脈と腹部大動脈瘤の治療を要しました。こうした症例を見るとつくづく動脈硬化は全身病であることを思い知らされると同時に心臓(ポンプ)以外の全身の動脈(パイプ)の病気を薬とメスとカテーテルを駆使し包括的に治療できる血管外科医あるいは動脈硬化外科医の重要性を再認識します。
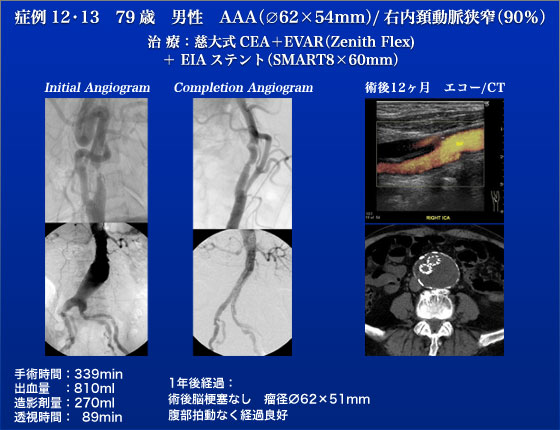
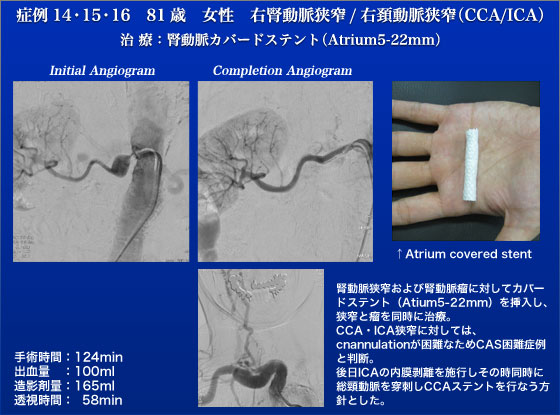
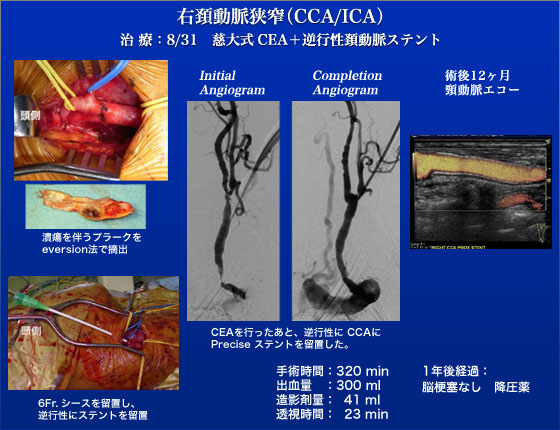
症例14、15、16は、81歳女性、右腎動脈狭窄、右腎動脈瘤、右総頸動脈狭窄、内頸動脈狭窄の症例です。高安動脈炎(大動脈炎症候群)の既往があり、多発病変の症例であります。降圧剤3剤を内服するも血圧コントロール不良な症例であり、右腎動脈狭窄、瘤に対して、カバードステント(Atrium AdvantaV12 5-22)を留置し、動脈瘤と狭窄を同時治療しました。最終造影はバッチグーと言える出来栄えでした。本症例は胸腹部大動脈瘤に対する枝付きステントグラフト同様、海外から未承認デバイスを輸入しないと治療が困難な症例です。頸動脈狭窄は鎖骨下の総頸動脈狭窄を伴うtandem lesionであったためステント術を予定しましたが術中造影で総頸動脈、内頸動脈の高度狭窄とともに総頸動脈の屈曲が強い事が判明致しました。本症例は手術不能例ではない上に、無理にステント術を行うと脳梗塞リスクが高い事から会場の皆さんと相談しながら後日、CEA/総頸動脈ステント術の方針としました。大勢の参加者がいるライブ手術では予定されていた治療をあきらめる事を躊躇してしまいがちですが、どの様な状況でも患者を第一に考える事が肝要である事は論を待ちません。JESの4日後の8月31日に、全身麻酔下に頸部を3cm切開し、右内頸動脈のCEAを施行しました。総頸動脈狭窄に対しては、CEA終了後にCEA部からステント(PRECISE 8-30,7-30)を留置しましたが、PTAとステント留置の際は総頸動脈を遮断し脳梗塞予防に努めました。脳梗塞などの合併症もなく元気に退院しました。術後約1年経過した現在でも、頸動脈、腎動脈とも再狭窄なく、経過良好であります。また、コントロール不良であった高血圧は極めて安定しています。大動脈炎症候群の症例では、再狭窄予防の観点からカバードステントは有効なオプションであると思われます。また、腎動脈瘤に対する治療も同時に出来ましたのでカバードステントは極めて合理的な選択でした。さらに、頸動脈の高度屈曲例に対しては様々なデバイスの挿入などに困難を伴い、脳塞栓のリスクも著明に上昇するため本法のようなハイブリッド治療が非常に有用です。こういったオプションが可能なのも内膜剥離術、頸動脈ステント術の両方を行なっているからでしょう。症例5で「インターベンションの治療においては術中の外科手術のリスク評価とそれに照らしてインターベンション追及のさじ加減を決める事が大事であることを本症例は教えてくれています」と書きましたがこのコメントは本症例にも言える事です。
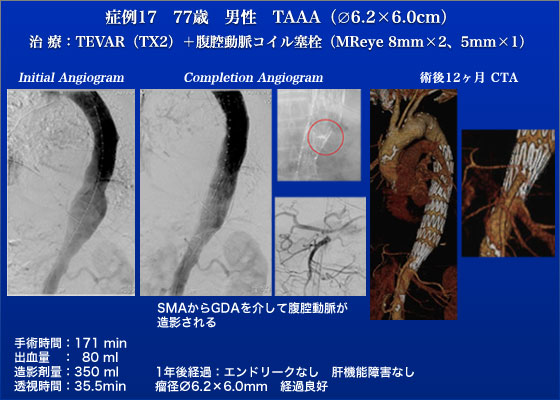
症例17は78歳の男性でCrawford I 型のTAAAです。Celiacは動脈瘤に巻き込まれていましたが、その末梢からSMA間にlanding zoneが存在し、また胃十二指腸動脈が開存していたため、celiacをcoverして胸部ステントグラフトを留置する予定としました。ここで使用したのが当時日本ではまだ未承認であったZenith TX2 ステントグラフトです。TX2 distal graftは、その末梢側にバーブの付いたbare stentを持ち、留置後のmigrationリスクが少なく、正確な留置、強固な固定を特徴としています。本症例ではCeliacのcoil塞栓を行うため、あらかじめ右上腕からKMPカテーテルを選択的にceliac内に留置しました。そしてproximal graftを、次いでdystal graftをSMA直上に留置しました。ここでSMAを選択的に造影すると、GDAを介してceliacからtype2 ELが見られたため、あらかじめceliacに留置していたKMPカテーテルよりMReye coilを用いceliacを塞栓しました。最終造影ではType1bエンドリークなく見事に瘤はTX2により空置されました。術後肝機能異常は見られず軽快退院されています。術後1年のCTでもエンドリークを認めず経過良好です。Crawford I 型に対しては開胸開腹手術の侵襲が極めて高いのでZenith TX2と腹腔動脈のコイル塞栓術が極めて有効です。ただ、腹腔動脈を犠牲にする前にCTAなどで胃十二指腸動脈の開存性をチェックしておくことが肝要です。
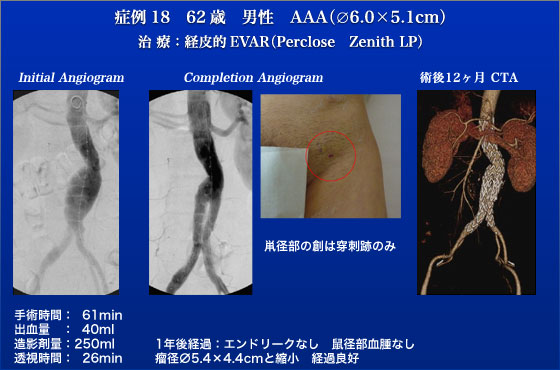
症例18はAAAに対して本邦初の次世代ステントグラフトであるZenith LPを使用した症例でした。Zenith LPはステントがステンレスからNitionolへ変わり、メインボディが外径16Fr(14Frシースに相当)と小口径となりました。したがってこの小口径を最大限アピールするために当日はPerclose を用いて局所浸潤麻酔下に経皮的に行ないました。ステントグラフトのシースを抜去したあともほとんど出血は認められず、ほぼ完全止血を得ることが可能でした。術後経過も良好で1年後のCTでは瘤径も著明に縮小しております。この後2011年2月より20例のZenith LPに対する日米共同治験を行ないましたが、全症例に局所麻酔下でPerclose ATを用いたEVAR治療を完遂しました。術後の穿刺部血腫はゼロであり、小口径のステントグラフトの威力を再確認しました。JES2010のハイライト症例です。
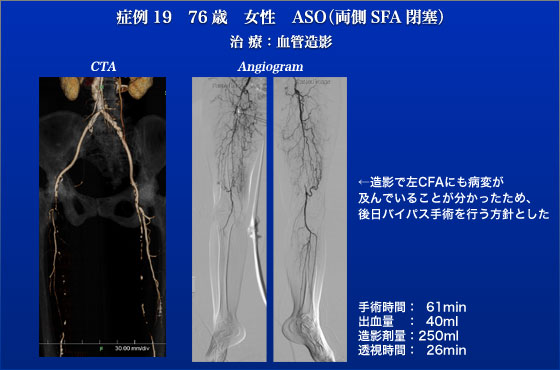
症例19は76歳の女性で両下肢の間歇性跛行50mということで当院にこられました。
もともとは近所に自分で買い物に行っていたのに行けなくなったことが一番のcomplaintでしたので治療適応と判断しました。術前CTでは両側のSFAの閉塞が見られ特に左はSFAの根部が残っており血管内治療のよい適応と判断して、Viabahn(Gore)を用いたいわば血管内FPバイパスと言うべきSFAステントを予定しておりました。しかしながら造影をしてみますと左総大腿動脈にも病変が進行しており後日FPバイパスを行う予定といたしました。結局JESの3日後の8月30日に両側のFPバイパスおよび総大腿動脈の内膜剥離とprofundaplastyを同時に行ない、元気に退院されました。退院後は念願だった買い物にも行けて幸せな日々を過ごしております。JESというと血管内治療の会の様にとらえられがちですが血管内治療は保存的治療(薬物療法や運動療法)、外科手術と並ぶ治療法の一つであることを強調したいと思います。こういった総大腿動脈や大腿深動脈にも病変を伴う症例においてはこれらの病変を同時に直すことが出来るバイパス手術を選択するべきであると思います。我々は通常術前血管造影を施行する事はほとんどありませんが、それはJES症例でも同じことで、本症例も術前血管造影をしておりませんでしたので稀にこうした読み違えが生じます。しかし、術前血管造影の負担は患者、医療者の両者にとって負担ですしメリット・デメリットの観点から正当化されないと考えています。
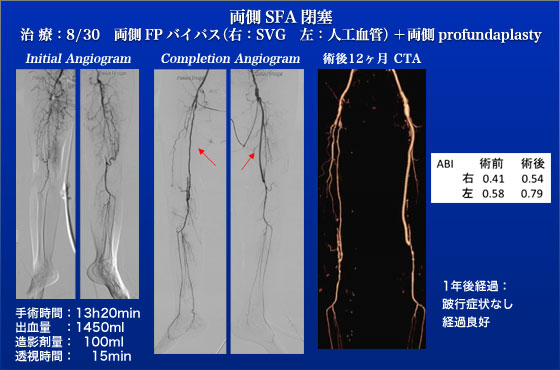
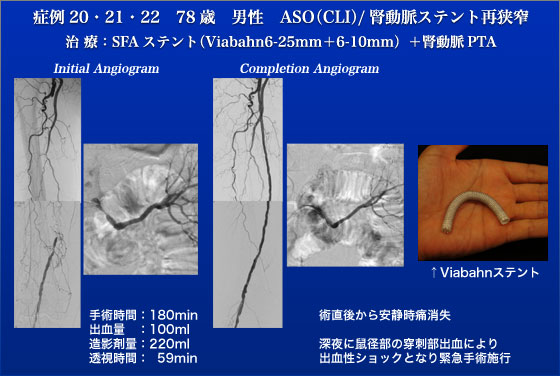
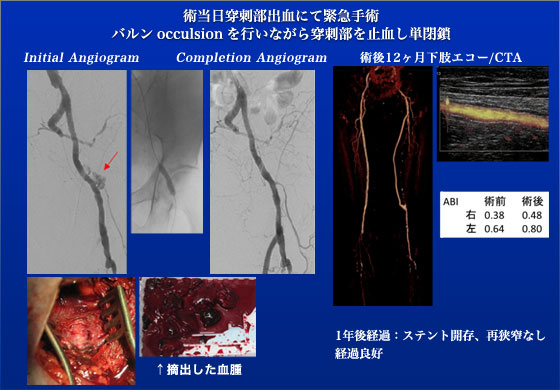
症例20、21、22は78歳男性で左下肢ASOに対して左F-Pバイパス(Distaflow施行歴あり、今回右下肢ASO(右母趾安静耳痛)に対して血行再建術施行となりました。CTAで右SFAの30cmと長い完全閉塞を認め通常であれば右F-Pバイパスの適応ですが、虚血性心疾患(CABG施行後)、脳梗塞の既往があることを考慮し今回局所麻酔で血管内治療を行いました。選択した方法は本邦初となるヘパリンコート付きのViabahnステントグラフト(20cm長)を閉塞SFA全域に留置するというものでした。30cmのCTO病変でしたがスムーズにワイヤで突破する事ができました。長い病変でしたがViabahnには20cmと長い物がありますのでステント2つで終了する事ができましたがこれもViabahnの長所の一つです。出来上がりのangioを見るとまるでF-Pバイパスを施行したかのような画像所見です。なお、残念ながらJES当日夜に左鼠径穿刺部の圧定解除後に鼠径部血腫のために出血性ショックとなり緊急止血手術を施行しました。対側から挿入したバルーンで左外腸骨動脈腸骨の閉塞をする事で血管コントロールをしつつ穿刺部を縫合閉鎖しましたが出血の原因はhigh punctureでした。幸い同側のF-Pバイパスは開存したままでした。1年後の経過ではViabahnステントは良好に開存、再狭窄や症状の再発は認めていません。これは従来のbare metal stentではあり得ない結果です。今後このViabahnステントグラフトの開存率がバイパスに匹敵するような成績を得られればASOに対する画期的な治療法が一つ誕生することになります。Viabahnについては今後TASC C/D病変を対象に国内で他施設共同治験を行う予定ですので皆様に協力をお願いするかもしれません。また、同時に“おまけ”として左腎動脈ステントの再狭窄のPTAを行なっております。下腿のPTA(症例22)も予定していましたが術中判断で不要と判断しました。1年後の経過をみてもこの判断は正しかった事が明らかです。
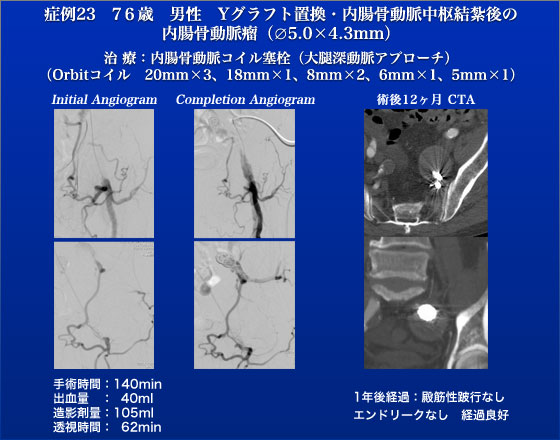
症例23は追加症例です。他院で腹部大動脈瘤人工血管置換術を受けた際に、左内腸骨動脈は分岐部(起始部)で結紮されていました。この残存する左内腸骨動脈がType II エンドリークにより瘤化し、1年で6mm拡大し50×43mmと巨大な症候性内腸骨動脈瘤となり、JES直前に紹介受診しました。下腹部痛を訴えていましたので準緊急手術の適応と判断しましたがJES前も後も予定が一杯だったので、苦肉の策としてJESの最後におまけ症例として治療する事にしました。左内腸骨動脈中枢側は結紮されており、アプローチ出来ませんので、左大腿動脈を順行性に穿刺し、左大腿深動脈経由で左内腸骨動脈瘤に到達し、コイル塞栓術を行う計画としました。Prowlerマイクロカテーテルにて左大腿深動脈から曲がりくねった下殿動脈経由で何とか左内腸骨動脈瘤に到達し、左内腸骨動脈瘤に流入している閉鎖動脈をOrbitマイクロコイル1本にて閉鎖し、左内腸骨動脈瘤内をOrbitマイクロコイル5本、下殿動脈をOrbitマイクロコイル2本にて閉鎖しました。術後、殿筋性跛行を認めず、退院となっています。術後半年のCTで明らかなリーク無く、左内腸骨動脈瘤は36mm大に縮小し、経過良好です。“おまけ”症例でしたが終わってみればJES 2010の最後を飾るにふさわしい、示唆に富んだ教育的な症例でしたし、来院後JES枠を利用してすぐに治療を受けられた患者にとっても有益だったと言えます。
JES 2010も皆様のご協力を得ながら大きな合併症もなく無事終了しました。第5回まで通算112例のライブ手術を行いましたが、死亡例はなく術中合併症も初年度の頸動脈ステント術の術中に生じた網膜梗塞の一例に限られています。毎年こうして全例を振り返っていますが、症例の内容、手技、出来栄え、会場の皆さんとのやり取り、のいずれをとっても最高に満足できるJESとなりました。JES 2011は皆さんのご協力を得ながら一層、質が高く安全なライブにしたいと願っています。
Japan Endovascular Symposium研究会
実行委員長 大 木 隆 生
![]() 医療ルネサンス(読売Online) [ 医療ルネッサンスTV / 頚動脈ステント術 / 大動脈ステントグラフト術 / 閉塞性動脈硬化症の治療 ]
医療ルネサンス(読売Online) [ 医療ルネッサンスTV / 頚動脈ステント術 / 大動脈ステントグラフト術 / 閉塞性動脈硬化症の治療 ]
![]() ニューズウィーク誌 [ Newsweek 2000-1.19 私たちが世界標準だ / 2006-10.18 世界が尊敬する日本人100人 ]
ニューズウィーク誌 [ Newsweek 2000-1.19 私たちが世界標準だ / 2006-10.18 世界が尊敬する日本人100人 ]
